克利夫兰诊所与IBM联合推出模拟蛋白质的新型量子工作流程
2026年3月23日——研究人员首次利用量子计算模拟了蛋白质的电子结构,这一突破性演示得益于新型量子中心超级计算(QCSC)研究。
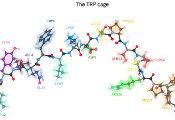
克利夫兰诊所与IBM联合研究团队采用量子中心超级计算工作流和IBM Quantum Heron r2量子处理器,成功对含303个原子的微型蛋白质Trp-cage进行建模。该成果源于量子-经典混合计算工作流设计及应用方面的进展,通过结合量子计算与高性能经典计算实现强大效能。
随着体系规模增大,经典计算机进行精确电子结构计算的难度呈指数级增长。虽然经典方法能有效模拟蛋白质某些特性,但对完整蛋白质进行高精度量子力学处理仍不现实。若量子计算机最终能精确建模具有生物意义的大分子,将深刻影响化学、材料科学和医学研究。本工作正是朝着该目标迈进的重要一步。
“能取得这一成果让我感到难以置信,”克利夫兰诊所Merz实验室负责人Kenneth Merz博士表示。
大分子建模的意义
Trp-cage是计算化学方法的重要基准测试体系。作为蛋白质它结构相对紧凑,却具备生物化学中大分子的典型特征:如疏水核心结构、组分间的氢键网络等,可形成复杂三维构象。该团队同时模拟了其折叠与非折叠(伸展与收缩)状态。
论文合著者Mario Motta指出:“在Trp-cage上验证该方法,是通向更大分子模拟的里程碑。”研究团队对现有成果也感到意外:“最初计划仅模拟几个氨基酸”,但随着工作流测试推进,他们发现能扩展至完整Trp-cage并获得有效结果。
Merz期待随着方法成熟,可支撑药物研发等领域的计算工作流。他设想未来科学家能利用QCSC工作流构建分子行为模拟数据库,通过机器学习筛选符合特定功能的分子结构,再通过实验验证。
大分子模拟新范式
该团队在arXiv预印本中描述的工作流采用基于波函数的嵌入方法(EWF),将Trp-cage分解为可计算的“簇”单元。EWF中每个原子对应一个簇,但每个簇包含该原子及其相互作用邻域,复杂度远超单原子。
蛋白质中不同簇的复杂度存在显著差异:位于边缘的原子可能仅与1-2个原子纠缠,可用经典方法高效求解;而分子核心区域的簇涉及复杂相互作用网络,正是量子计算机的优势领域。通过整合各簇计算结果,最终获得描述电子分布及相互作用的完整分子电子结构——这是决定分子行为的关键信息。这种量子-经典混合工作流展现了量子中心超级计算的雏形。
面向HPC的新一代量子中心算法
Merz见证量子计算多年发展,早期虽知其能解决化学难题,但具体路径尚不明确。转折点出现在看到IBM科学家提出的样本量子对角化(SQD)算法时——这属于专为量子中心超级计算设计的新算法族,通过协同发挥量子与经典计算优势解决问题。
SQD针对电子结构计算的核心挑战:分子电子构型数量随分子尺寸组合爆炸。量子计算机通过采样筛选关键构型,经典计算机据此聚焦求解。Merz团队立即全力投入SQD研究,从测试小分子起步,最终完成Trp-cage模拟。目前该工作流精度已媲美最严苛的经典计算方法。
科学家指出EWF-SQD联合工作流理论上可远超Trp-cage规模。虽然大分子分块计算与重组更复杂,但量子计算机处理复杂簇电子结构的优势明显。团队已着手瞄准更大分子目标。
QCSC发展需要量子计算与HPC领域深度协作。本研究利用了密歇根州立大学和克利夫兰诊所的HPC资源,IBM与RIKEN等机构的近期合作也取得显著成果。